健康保険が適応(適用)になる標準治療(手術、放射線療法、抗がん剤)は、「がんを攻撃する」ことだけを意識して設計されました。「目」で見ることができ手術で取り除くことができる大きな腫瘍の塊、画像診断で検出可能な顕著で大きな腫瘍組織、目に見えるものを潰せばいい、そうした考え方からがん治療の基本設計がなされてしまいました。ところが、がんの正体は小さながん細胞が集まったものです。しかも画像に全く映らない小さながん細胞(特にがん幹細胞という腫瘍の種になるもの)が飛び散りやがて大きな腫瘍をつくります。患者さんの命を奪う悪性度の高いがん、つまり活発に転移したり再発を繰り返すタイプのがん細胞が体内にいる場合は、たとえ画像に映らず腫瘍マーカーが正常値であっても危険な状態です。特に方々へ飛び散る性質をもつがんが勢いを得れば、あっという間に全身の様々な部位に腫瘍をつくり手に負えなくなります。
一方、がん細胞にとって目の上の瘤は体内の免疫システムです。放射線や抗がん剤で大きな腫瘍を叩いても、治療の副作用で免疫システムに打撃を与えてしまうと、結局がんの勢いが強くなってしまいます。なお、標準治療のエビデンス(効果の証明)というのは腫瘍への打撃だけを測定し、がんを抑える要である免疫システムへの打撃という副作用は最初から測定していません。一時的な測定しやすい効果だけで有効と判断されたものです。
標準治療の代表格、外科手術は局所療法です。放射線や重粒子・陽子線療法も局所療法です。問題は、見えなかっただけで小さながん細胞が手術前に飛び散っているケースです。手術で全部取れたと思ってもやがて再発や遠隔転移となります。 外科手術は分散してしまった微小がんには対応できません。放射線も全身照射はできません。再発や遠隔転移となれば、基本的な治療法として抗がん剤を使うしかありません。
さて、体内の2箇所以上にがんと考えられる腫瘍があるだけで原則、手術不能と判断されます(手術する場合もあります)。沢山の腫瘍が方々にあれば手術できないのは仕方ないですが、なぜ2個しかないのに2箇所とも手術で取り除いてくれないのでしょうか。
放射線療法や、抗がん剤は、がん細胞と正常細胞を区別することなく、増殖(細胞分裂)中の細胞の遺伝子にダメージを与えます。 ところが、がん細胞のすべてが同時に細胞分裂していることはありません。必ず、生き残るがん細胞がいます。また、免疫細胞を始め、多くの正常細胞が、がん細胞より増殖が活発で、がんよりも先に打撃を受けてしまいます。そのため、放射線療法や抗がん剤を際限なく続けると、患者さんは生命維持さえ困難となります。延命を目的に実施されるもの であり、治癒は最初から想定されていません。
全身療法である抗がん剤には副作用の激しい殺細胞性化学療法剤、ホルモン療法剤、分子標的薬などがあります。現在、日本で使われている抗がん剤の代表格は殺細胞性化学療法剤です。日本では、一般に、抗がん剤といえば、殺細胞剤だけのことを意味する傾向がありますのでここでも「抗がん剤」=「殺細胞剤」として扱います。世界全体ではがん治療薬といえば分子標的薬のことであり、殺細胞剤は1~2割程度に過ぎません。
抗がん剤は、増殖毒と言われ、増殖中(細胞分裂中)の細胞の遺伝子に傷をつけます。がん細胞と正常細胞を区別することはできません。増殖中であればどちらも攻撃します。体内には、がん細胞よりも早く増殖する正常細胞が多く存在し、先にやられてしまいます。そのため、激しい副作用は避けられません。ただし、白血病の場合、がん細胞の増殖が極めて速く、固形がんより効率よくがん細胞に打撃を与えられることもあります。
標準治療の考え方は、進行がんは治癒できない、という前提に立ち、一時的な「効果」を求めるか「延命」を求めるものです。
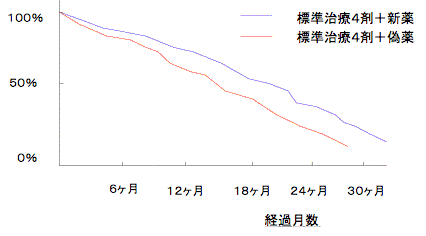
今日では「縮小効果による奏効率」に代わって、「延命効果」が抗がん剤の効果判定基準として用いられています。末期進行がんの患者さんにおいて、既存の抗がん剤を投与したグループと、既存の抗がん剤+新薬を投与した場合を比較し、どれだけ生存期間が延びたか、を判定するものです。例えば、前者の余命が14.5ヶ月に対し、後者の余命が16.0ヶ月であれば、1.5ヶ月の延命効果を認められ承認となります。
典型的な延命効果試験の結果
実は、最新の抗がん剤のエビデンスといっても、2~3ヶ月以下の延命効果を示しているに過ぎません。しかも、標準治療を受けなかった場合との比較試験は行われていません。科学的には、問題の多いエビデンスということになります。
分子標的薬とADCC活性
「抗がん剤との併用」では、免疫細胞療法がフェアな評価を受ける治験を設計することはできません。
標準治療は、大きな腫瘍の塊を除去する、大量増殖中のがん細胞の総数をざっくり減らすことは得意です。ところが、全身に散る危険ながん細胞を根絶することが苦手です。放射線や抗がん剤は、がん幹細胞を叩くのが苦手 です。むしろ、中途半端に傷をつけるため、かえって活発な転移を促進すると指摘されています。ダラダラ続けると合併症ばかりが悪化していきます。
標準治療は絶対駄目なんだ、と決めてかかる患者様にANK療法実施医師が、手術、放射線、抗がん剤などとの併用を薦めると、大変驚かれることもあります。ANK療法実施医師は、基本的に標準治療の邪魔をしない治療設計を考えます。まずは標準治療を続けながら、少しでも早い段階でANK療法実施医師に相談されることをお勧めします。理想的には抗がん剤投与前にANK療法によるNK細胞の培養を済ませておけば、抗がん剤によるダメージを回避したNK細胞を治療に使うことができます。