がんの塊に短期間で打撃を与えられる局所療法(手術、放射線など)は、できる限り実施します。
但し、標準治療で打撃を受ける前に、リンパ球を採取し、標準治療実施中に、ANK療法の培養を行うことが理想的です。日程的に無理があれば、手術などの局所療法は予定通り実施し、その後、ANK療法の培養を行います。手術不能の場合は、先にANK療法を実施し、症状の改善がみられ、手術可能な状態になれば、速やかに手術を行うことが推奨されています。
全身療法の中でも、免疫と相性がいい分子標的薬や、ホルモン療法は極力、ANK療法と同時併用します。免疫とは相性は悪いものの、増殖の速いがんの勢いを削ぐのが得意な殺細胞性化学療法剤(一般的な抗がん剤)については、ANK療法と時期をずらして行います。
抗がん剤(化学療法剤、殺細胞剤)とANK療法の同時併用は推奨されません。
抗がん剤(殺細胞性)は、正常細胞の遺伝子にも傷をつけます。
そのため、薬剤投与直後は、血液中の薬剤濃度が高く、点滴で戻したNK細胞も強く傷害を受けてしまいます。
また、抗がん剤によって、一時的に異常細胞と化した正常細胞を、NK細胞が攻撃する可能性があります。
ANK療法は、免疫刺激作用が強く、体内の免疫反応を誘導し、がんによって眠らされた体内の免疫細胞の活性化も促します。免疫反応は基本的に炎症反応ですので、免疫細胞の活動に伴って、炎症系のマーカーなどが一時的に上昇することがあります。たとえば、CRP値などが上昇すると、抗がん剤の副作用が激しいと判断され、抗がん剤治療が中止になるかもしれません。実際には、ANK療法により、検査数値が上昇しても、すぐに元に戻るので問題はないのですが、混乱を避けるためにも、点滴の時期は、体内の抗がん剤濃度が低下したタイミングで行います。薬剤によって、投与後、3日~10日程度の間を空けてから点滴するのが一般的です。
局所にある腫瘍組織に対する外科手術や重粒子線、また、増殖の活発ながんに対する抗がん剤(殺細胞剤)や放射線療法は、弊害はあるものの、初期の打撃力は絶大です。
一方、ANK療法では、がん細胞を一つずつ破壊していくため、相手が大軍であったり、破壊するがん細胞よりも、増殖するがん細胞の数が上回ったりすると、がんの勢いに押されてしまいます。
そこで、標準治療などにより、がん細胞の総数をざっくり減らし、後からANK療法を実施することは、治療効率を高め、費用対効果の改善につながります。
手術不能例で、危険な部位に浸潤している腫瘍組織をANK療法で小さくしてから、手術をする、ということもありますが、基本は、先にANK療法の培養・凍結保管、次に標準治療 後から ANK療法の点滴です。
ANK療法を実施後に、放射線療法や抗がん剤投与実施すると、免疫力が打撃を受け、低下した状態で治療を終えることになり、再発や転移の可能性が高くなると考えられます。最後の詰めは、がん細胞を全滅に追い込める正確ながん認識能力をもつNK細胞を用い、かつ、残ったがん細胞の増殖を抑えるだけの免疫レベルを回復した状態で治療を終えることが推奨されます。
大事なことは、先ず、ANK療法担当医に相談し、標準治療のスケジュールをベースに、ANK療法を含め、可能性があるすべての標準+先端治療全体の設計を立ててもらうことです。何か一つの治療をやって、駄目だから、次をやる、という泥縄式は、最適な治療の組み合わせを選択する機会を失い、費用ばかりかかって、症状を悪化させるだけです。標準治療をやりつくしてから、他の治療を探し始めたのでは、後手に回ります。その場合でも、できることの最善を尽くすのが医療ですが、進行がんの治療は先手を打つことが何より重要です。納得の上で、治療設計を組み立てれば、あとは、迅速に迷わず方針を貫くのが、治療効果を最大限に引き出す道と考えます。
非常に単純化したモデルで説明します。
例えば、総数で1000億個のがん細胞があったとします。
この内、990億個は、大きな腫瘍の塊として存在し、
残りは、全身に散っています。
外科手術や重粒子線は、990億個の腫瘍を一度に排除できますが、
残りは手をつけられません。
手術により、免疫を低下させ、また、大量の細胞増殖因子の分泌を招くと(傷つき、失われた組織を埋めるため、大量の細胞増殖を促すため)、残りの10億個のがん細胞が猛烈に増殖します。
もし、平均10日に一回の割合で、1個のがん細胞が2個のがん細胞に増えるペースになってしまったとすると、10億個のがん細胞は、一ヶ月で100億個、二ヶ月で1000億個に増えてしまいます。これでは、手術で取った意味がありません。実際には、がん細胞の分裂スピードは様々であり、僅かなスピードの違いが、増殖カーブとしては、大きな違いとなります。
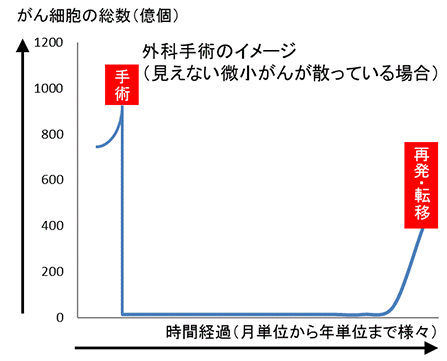
放射線療法の一定線量の照射や、抗がん剤1クールで、がん細胞の2割を破壊できる、と仮定します。効果の現れ方が、その時のがん細胞総数に対して、「割り掛け」になっていることに、ご注目ください。なお、薬剤耐性や、放射線の照射限界後は、がん細胞が増殖に転じます。
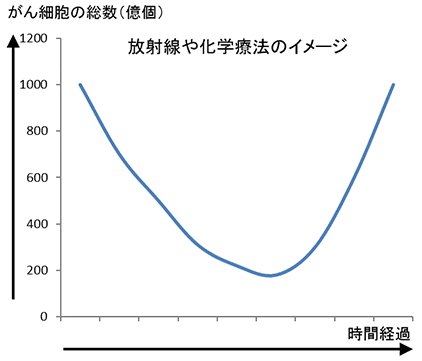
ANK療法は、仮に1クールで100億個のがん細胞を破壊する、とします。(実際には、毎回、同じ数のがん細胞を破壊する、と決まっているわけではありません、あくまで、仮の設定です)
体内に眠る大量のNK細胞が目を覚ませば、一気に大きな腫瘍の塊であっても撃破する可能性がありますが、ここでは、先ず、培養細胞が、直接、がん細胞を攻撃する効果だけを反映させます。
「引き算」で効いていることに、ご注目ください。
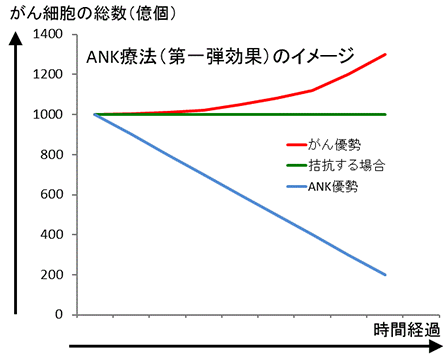
ANK細胞が、がん細胞を破壊する間、がん細胞も数を増やそうとしています。がん細胞が、ANK細胞によって、破壊されるペースを、がん細胞の増殖が上回れば、全体的にがんは増殖を続けてしまいます。一方、ANK細胞の勢いが上回れば、がん細胞の総数は減少を続けます。
放射線療法や、抗がん剤は、がん細胞の勢いが強いほど、がんに大きな打撃を与え、逆に、ある程度、数を減らしたあとの詰めができません。ANK療法は、優勢ながんに押されると、がん細胞の増殖を許してしまいますが、優位に立つと、薬剤耐性や、許容線量の制限といった問題や制約がありませんので、最後まで、詰めができます。
手術後に、再発防止として放射線・抗がん剤、あるいは、ANK療法をそれぞれ実施した場合はどうなるでしょうか。
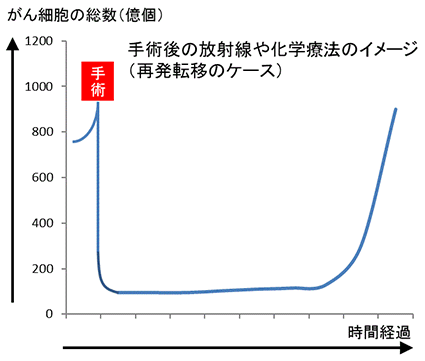
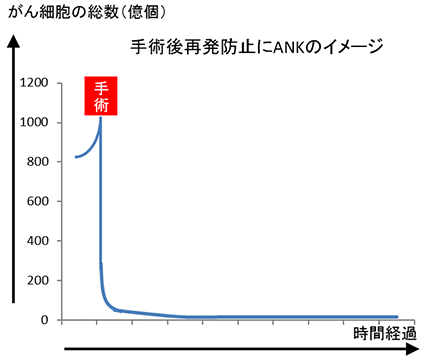
ANK療法の培養・凍結保管のあと、標準治療を前、ANK療法の点滴を後ろ、と、完全に分けてしまうパターンの他に、「合間治療」と呼ばれる方法があります。
抗がん剤投与を受ける前に、理想としては先にリンパ球を採取し、細胞を培養しておきます。抗がん剤投与は、ほとんどの場合「休薬期間」、つまり、抗がん剤の投与をお休みする期間がありますので、その間にANK細胞の量を減らし、投与間隔を空けて、点滴する、というものです。休薬期間中に、正常細胞の回復を待つのですが、がん細胞も増殖してしまいます。この期間、標準治療では、何の治療もできませんので、ANK療法による攻撃を加える、という意図と、少しでも、免疫系への打撃を回復しておく、という狙いがあります。但し、折角ANK療法を実施しても、その後直ぐに抗がん剤を投与すれば、抗がん剤によって、NK細胞は打撃を受けますので、貴重なANK細胞の使用は、控え目に行います。
「合間治療」における、最大のポイントは、抗がん剤投与を中止し、ANK療法による全力攻撃に切り替えるタイミングです。抗がん剤がよく効いている間は、がん細胞の数を減らせるだけ減らした方が、ANK療法の効果が出易くなります。ところが、タイミングをはずすと、取り返しがつかなくなります。薬剤耐性が現れると、もう抗がん剤の効果はガタ落ちになります。副作用の方は激しくなってきます。合併症が頻発し、重度を増してくると、治療継続が困難になり、休薬期間もはっきりしなくなると、ANK療法の合間治療ができなくなっていきます。更に抗がん剤を引っ張り続けると、がん細胞は増殖し、合併症は酷くなるという最悪の事態に陥り、そこからANK療法に切り替えても、がんの勢いは凄まじいものがあります。
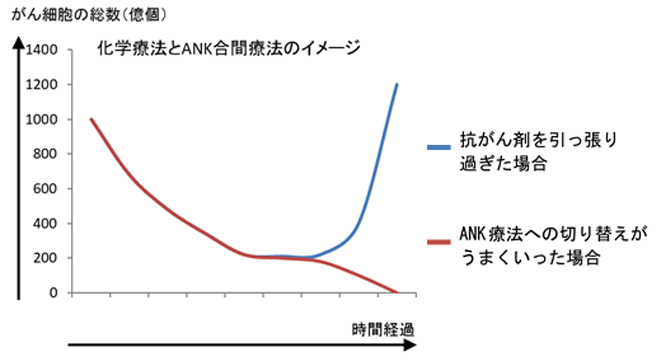
上記のグラフは、あくまで、基本的な考え方をご理解いただくための、仮定に基づくイメージ図です。実際の治療データではありませんので、誤解のないよう、お願い申し上げます。







